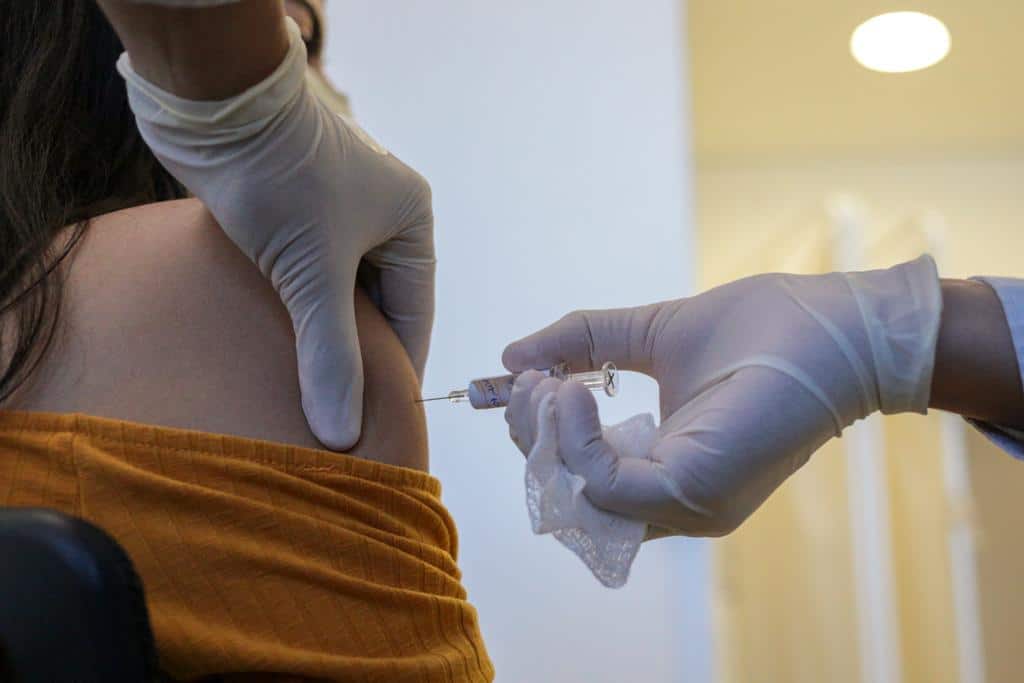
A Agência Nacional de Vigilância Sanitária (Anvisa) anunciou na noite de segunda-feira (9) a suspensão temporária dos estudos clínicos da vacina contra o novo coronavírus desenvolvida pela farmacêutica chinesa Sinovac Biotech. A decisão foi tomada após a ocorrência de um “evento adverso grave” relacionado com a CoronaVac não informado pela Anvisa. Em nota, a agência apenas apontou que são considerados “eventos adversos graves” casos de óbito, eventos que comprometam a saúde do voluntário, incapacidade ou invalidez, reações que demandem hospitalizações, anomalias e suspeitas de infecção por meio de agentes. “Com a interrupção do estudo, nenhum novo voluntário poderá ser vacinado. A Anvisa reitera que, segundo regulamentos nacionais e internacionais de Boas Práticas Clínicas, os dados sobre voluntários de pesquisas clínicas devem ser mantidos em sigilo, em conformidade com princípios de confidencialidade, dignidade humana e proteção dos participantes”, destacou o órgão.
PATROCINADORES